Учебник по Физике.
Оглавление учебника
Электропроводность различных веществ.
Электропроводность различных веществ определяется типом носителей тока и свойствами среды, в которой распространяется ток. Детальное рассмотрение механизма электропроводности возможно только на микроскопическом уровне, а следовательно, с помощью законов квантовой механики атомов и молекул.Электропроводность проводников (металлов). Вольт-амперная характеристика металлов имеет типичный вид, соответствующий закону Ома I = U/R. Такая зависимость сохраняется в очень широком диапазоне температуры.
Температурная зависимость сопротивления. Для большинства чистых металлов удельное сопротивление линейно зависит от температуры:
Здесь r0 - значение удельного сопротивления при некоторой выбранной температуре T0, a - температурный коэффициент сопротивления, [a] = K-1. Численно этот коэффициент для всех металлов порядка 10-3 К-1. Иными словами, сопротивление металлов слабо зависит от температуры практически во всем диапазоне допустимых температур от точки плавления до сверхнизких.
У некоторых металлов (например, ртуть, олово) сопротивление внезапно падает до нуля при охлаждении ниже некоторой критической температуры Тс. Это явление получило название сверхпроводимости. Типичные температуры перехода в сверхпроводящее состояние у металлов очень малы (< 20 К).
Электрический ток в жидкостях. Водные растворы электролитов проводят ток. Носителями тока являются ионы электролита, образовавшиеся в результате разложения молекул электролита в водном растворе. В растворе электролита непрерывно конкурируют процессы диссоциации и обратной рекомбинации ионов в молекулы электролита. При заданной температуре устанавливается динамическое равновесие и среднее число ионов обоих знаков не изменяется. Степень диссоциации (доля молекул электролита, распавшихся на ионы) растет с ростом температуры, поэтому в нагретом электролите концентрация положительных и отрицательных ионов увеличивается.
Закон электролиза. Ионы - проводники тока в растворе электролита - попадают на электроды и, отдавая, либо получая электроны, превращаются в атомы соответствующих веществ. Процесс выделения вещества на электродах при пропускании тока через раствор электролита называется электролизом.
Пусть m0i - масса отдельного иона, q0i = ne - его заряд (n - валентность иона, е - величина элементарного заряда), а Ni - число ионов, попавших на электрод за время Dt. Полный заряд, прошедший за это время через электролит, равен Dq = IDt, поэтому
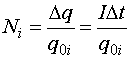
Масса вещества, выделившаяся на электроде, равна
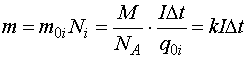 (15.2)
(15.2)Коэффициент
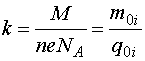
носит название электрохимического эквивалента. Эта величина различна для разных веществ.
Полученная формула (15.2) представляет основной закон электролиза (закон Фарадея):
Масса вещества, выделившегося на электроде, прямо пропорциональна количеству заряда Dq, протекшему через раствор электролита. Постоянная величина QF = eNA = 96500 Кл называется постоянной Фарадея. При прохождении количества заряда QF на электроде выделяется количество вещества, равное массе одного моля вещества, деленной на валентность иона-носителя.